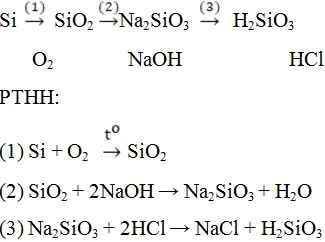Tìm hiểu về Phản ứng giữa Carbon và Hydro
Trong lĩnh vực hóa học, phản ứng giữa carbon và hydro đóng một vai trò quan trọng trong việc sản xuất và sử dụng các hợp chất hữu cơ. Một trong những sản phẩm nổi bật nhất của phản ứng này là metan (CH4), một loại khí tự nhiên có ứng dụng rộng rãi trong nhiều lĩnh vực. Bài viết này sẽ khám phá chi tiết về phản ứng giữa carbon và hydro, từ cấu trúc hóa học đến ứng dụng thực tiễn của sản phẩm tạo thành.
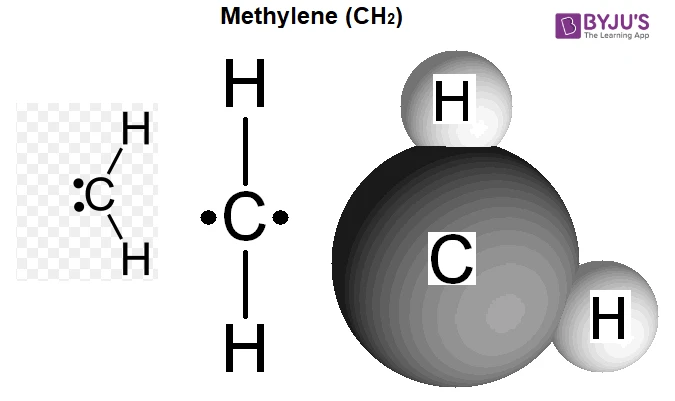
1. Phản ứng Hóa Học giữa Carbon và Hydro
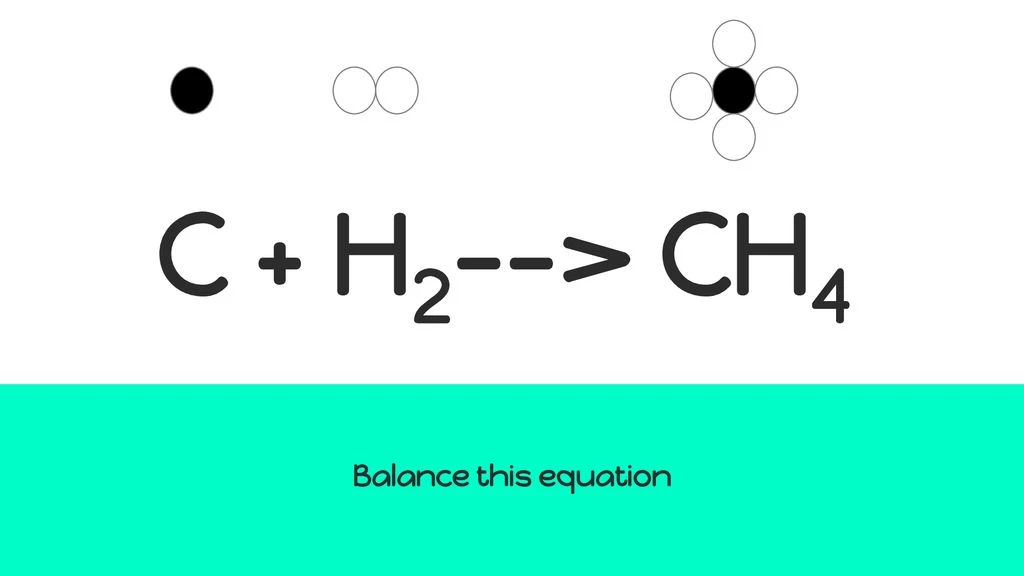
Phản ứng giữa carbon và hydro có thể được mô tả bằng phương trình hóa học đơn giản: C + 2H2 → CH4. Để hiểu rõ hơn về phản ứng này, trước tiên chúng ta cần xem xét các thành phần tham gia:
- Carbon (C): Là một nguyên tố phi kim, carbon có khả năng kết hợp với nhiều nguyên tố khác để tạo ra các hợp chất hữu cơ.
- Hydro (H2): Là một khí không màu, không mùi, hydro là một trong những nguyên tố phổ biến nhất trong vũ trụ và thường được gặp dưới dạng phân tử H2.
Phản ứng này được gọi là phản ứng tổng hợp, trong đó hai nguyên liệu đơn giản (carbon và hydro) kết hợp với nhau để tạo ra một hợp chất phức tạp hơn (metan).
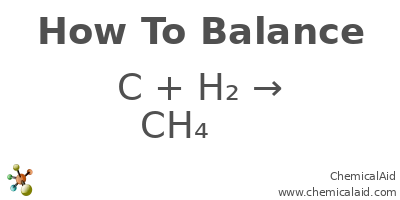
2. Quá Trình Cân Bằng Phản Ứng
Cân bằng phản ứng hóa học là một bước quan trọng để đảm bảo rằng số lượng nguyên tử của các nguyên tố ở cả hai bên của phương trình là như nhau. Đối với phản ứng giữa carbon và hydro, chúng ta cần đảm bảo rằng có đủ lượng hydro để phản ứng với carbon. Bằng cách cân bằng phương trình, chúng ta có:
C + 2H2 → CH4
Điều này có nghĩa là một mol carbon cần hai mol hydro để tạo ra một mol metan. Khi hiểu rõ về tỷ lệ này, chúng ta có thể tính toán lượng nguyên liệu cần thiết cho các ứng dụng thực tế.
3. Ứng Dụng của Metan
Metan là một trong những nguồn năng lượng quan trọng nhất ngày nay. Dưới đây là một số ứng dụng chính của metan trong đời sống hàng ngày và công nghiệp:
3.1. Nguồn Năng Lượng
Metan, như một loại khí tự nhiên, thường được sử dụng làm nhiên liệu cho các thiết bị sưởi ấm, nấu ăn và sản xuất điện. Nó là một nguồn năng lượng sạch hơn so với than đá và dầu mỏ, góp phần giảm thiểu ô nhiễm môi trường.
3.2. Nguyên Liệu Hóa Học
Ngoài việc sử dụng làm nhiên liệu, metan còn là nguyên liệu đầu vào cho nhiều quá trình hóa học, bao gồm sản xuất amonia, methanol và các hợp chất hữu cơ khác. Các sản phẩm này có vai trò thiết yếu trong ngành công nghiệp hóa chất.
3.3. Chất Khử trong Các Phản Ứng Hóa Học
Metan có thể được sử dụng như một chất khử trong nhiều phản ứng hóa học. Ví dụ, trong sản xuất kim loại từ quặng, metan có thể giúp loại bỏ oxy từ oxit kim loại.
4. Tính Chất Hóa Học và An Toàn
Mặc dù metan có nhiều ứng dụng hữu ích, nhưng nó cũng cần được sử dụng cẩn thận. Dưới đây là một số điểm quan trọng về tính chất hóa học và an toàn khi làm việc với metan:
4.1. Tính Chất Hóa Học
Metan là một hợp chất ổn định và không độc hại, nhưng nó có khả năng cháy rất mạnh. Khi châm lửa, metan sẽ tạo ra một ngọn lửa xanh đặc trưng, điều này có thể dẫn đến nguy cơ cháy nổ nếu không được sử dụng đúng cách.
4.2. Nguy Cơ và Biện Pháp An Toàn
Khi làm việc với khí metan, cần chú ý đến các nguy cơ tiềm tàng như rò rỉ khí, có thể gây ra nổ. Để đảm bảo an toàn, cần kiểm tra thường xuyên các thiết bị và ống dẫn khí, sử dụng các công cụ phát hiện khí rò rỉ, và đảm bảo thông gió tốt trong không gian làm việc.
Kết Luận
Phản ứng giữa carbon và hydro không chỉ là một trong những phản ứng hóa học cơ bản mà còn có nhiều ứng dụng trong cuộc sống hàng ngày và công nghiệp. Từ việc cung cấp nguồn năng lượng sạch đến việc sản xuất các hợp chất hữu cơ quan trọng, metan đã chứng minh được giá trị và tầm quan trọng của nó trong xã hội hiện đại. Hiểu rõ về quá trình phản ứng, tính chất và ứng dụng của metan sẽ giúp chúng ta sử dụng nguồn năng lượng này một cách hiệu quả và an toàn hơn.
Việc nắm vững kiến thức về phản ứng giữa carbon và hydro sẽ không chỉ hỗ trợ trong nghiên cứu và học tập mà còn góp phần vào sự phát triển bền vững của nguồn năng lượng trong tương lai.